
取消
清空記錄
歷史記錄
清空記錄
歷史記錄



海藻糖這款藥用輔料的性質及生產工藝是怎樣的?
?說到海藻糖這款藥用輔料,本期AVT小編給大家詳細介紹一下海藻糖的性質及生產工藝,感興趣的小伙伴速來圍觀。

?▲ 海藻糖(供注射用)(無菌)
?AVT海藻糖產品信息
?1、產品名稱:海藻糖(供注射用)(無菌)
?2、中文名稱:D(+)-海藻糖二水合物
?3、英文名稱:D(+)-Trehalose dihydrate (for injection)
?4、化學名稱:α-D-吡喃葡萄糖基-α-D-吡喃葡糖苷二水合物
?5、分子式:C12H22O11·2H2O
?6、CAS號:6138-23-4
?7、分子量:378.33
?8、EINECS登錄號:202-739-6
?9、級別:無菌藥用輔料
?10、備案登記號:F20190000452
?11、DMF號:034401
?12、性狀:本品應為白色或類白色結晶性粉末,無臭,味甜,易溶于水,溶于熱乙醇,微溶于甲醇,不溶于乙醚、丙酮
?13、保存:密封、涼暗干燥處保存,常溫條件下運輸。
?海藻糖規格型號
?型號1、海藻糖(供注射用)無菌
? ? 無菌注射級,超低內毒素
? ? 備案登記號:F20190000452
? ? 包裝規格:3kg/桶,鋁桶
? ? 貨號:O08001
型號2、海藻糖(供注射用)
? ? 注射級,低內毒素
? ? 包裝規格:10kg/桶,紙板桶
? ? 貨號:O08002
?醫學上已成功應用海藻糖作為血液制品、疫苗、細胞組織等生物活性物質的穩定劑,這樣不僅可以延長常溫下的存放時間,更可以防止血源污染。同時海藻糖作為凍干保護劑在生物制品上的應用也很廣fan,與蔗糖相比能對蛋白起到更好的保護作用。
?AVT海藻糖具有低內毒素、無菌的品質高特點,滿足生物制品,血液制品和脂質體等各種高端注射劑開發需求。在我司注冊團隊的不懈努力下已獲得登記號(F20190000452),DMF(34401),助力客戶制劑產品中外申報(符合各國藥典標準Chp,USP,JP,EP )。AVT海藻糖具有超高性價比,提高客戶制劑產品競爭優勢。
?海藻糖的基本性質
?海藻糖是是一種穩定的非還原性雙糖,由兩分子葡萄糖以一個α,α,1,1-糖苷鍵構成。海藻糖最初是從黑麥的麥角菌中提取的,隨后發現它在自然界的動植物和微生物中廣fan存在,尤其在真菌、水藻、苔蘚和無脊椎動物中含量較高。海藻糖是白色晶體,一分子海藻糖含有兩分子結晶水,能溶于水、冰醋酸和熱乙醇,不溶于乙醚、丙酮。當加熱至130℃時,海藻糖失去結晶水變成無水晶體。其它性質見下表:
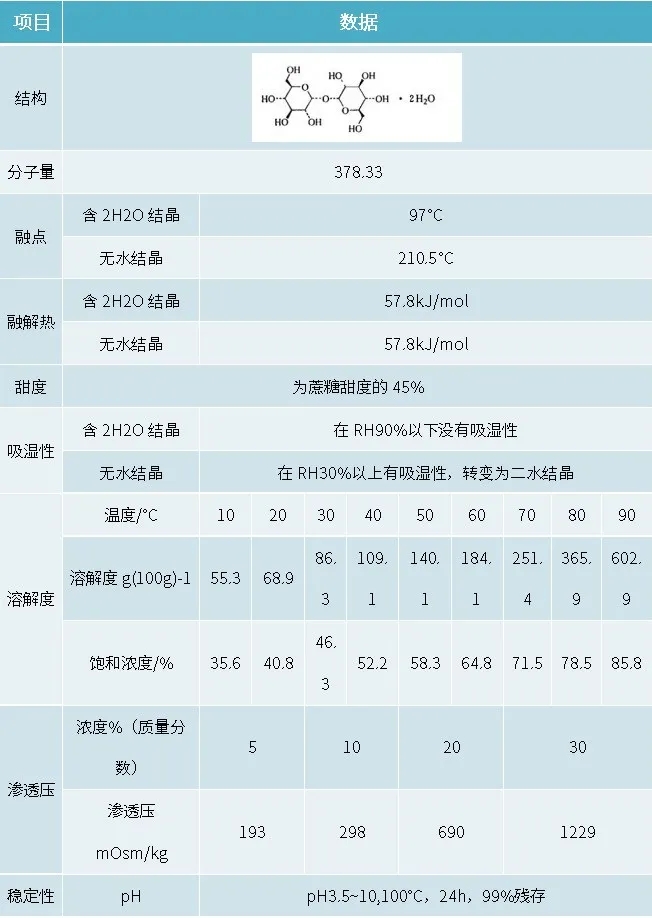
?海藻糖對生物體具有神奇的保護作用:其在高溫、高寒、高滲透壓及干燥失水等惡劣條件下能在細胞表面形成一層獨特的保護膜,有效的保護了細胞、蛋白質分子等不變性失活。而自然界中如蔗糖、葡萄糖等其它糖類則不具備這一功能,因此海藻糖在科學界還有個別名叫“生命之糖”。
海藻糖來源及工業化
?海藻糖廣fan存在于低等蕨類植物、藻類、細菌、真菌、酵母、昆蟲及無脊椎動物中,特別是在酵母、霉菌等真菌中,含量可高達生物體干重的20%以上。如何將其提取利用,甚至實現大規模工業化生產,人們做了大量的研究工作。目前海藻糖的制備方法包括化學合成法、微生物提取法、微生物發酵法、酶合成法、基因工程法等。
?微生物提取法
?以酵母、乳酸菌、霉菌及其它含海藻糖的微生物為提取源,首先通過改變微生物的生長條件,使其體內積累更多的海藻糖,然后采用適當的方法將海藻糖提取出來。微生物提取法生產海藻糖生產周期長,提取率低,成本高,很難實現大規模工業化生產。
?微生物發酵法
?通過微生物發酵生產海藻糖,再從發酵液中提取純化。其關鍵是通過誘變、細胞融合及基因重組等方法選育高產海藻糖的菌株。日本味之素公司,利用氨基酸生產菌體外培養大量生產海藻糖,已實現工業化生產,但該法轉化率低、副產物多。
?酶合成法
?以葡萄糖、麥芽糖、淀粉為底物,三種方法,但存在消耗高能,且磷酸化酶不穩定等問題,因而也難以實現工業化生產。
?基因工程法
?將海藻糖合成酶的基因導入植物或微生物,可利用工程微生物或轉基因植物生產海藻糖。
?化學合成法
?2,3,4,6 -四乙酰基葡糖和3,4,6-三乙酰-1,2-脫水-D-葡糖之間產生環氧乙烷加成生成。該法制備海藻糖的缺點是產率低、分離困難,目前還處于研究階段。
?哪些影響海藻糖質量因素
?海藻糖作為藥用輔料能穩定細胞膜和蛋白質的結構,有效地保護細胞膜和蛋白質分子不變性失活,從而維持生命體的生命過程和生物特征。隨著生物醫藥的發展,海藻糖作為一種優良的保護劑和穩定劑,應用變得廣。
?海藻糖作為藥用輔料,已經被收錄入多個國jia藥典中,比如NF35,EP9.0和JP17,CP2015。與口服給藥途徑相比,注射給藥途徑的海藻糖在一些質量指標上有更高的要求,如酸根離子、可溶性淀粉、有關物質等。隨著注射劑一致性評價的實施,由于注射劑生產中不允許再使用活性炭控制熱原(細菌內毒素),因此對原輔包的內毒素要求也會進一步提高。另外,無除菌工藝的制劑,還可能對海藻糖提出無菌的要求。
制劑如何變更海藻糖供應商
?國jia藥監局關于進一步完善藥品關聯審評審批和監管工作有關事宜的公告(2019年 第56號)已于2019年8月15日正式生效。對于上市藥品制劑變更輔料供應商的規定,可參見該公告(十七)條“已上市藥品制劑變更原輔包及原輔包供應商的,應按照《已上市化學藥品變更研究技術指導原則(一)》? 《已上市化學藥品生產工藝變更研究技術指導原則》《已上市中藥變更研究技術指導原則(一)》及生物制品上市后變更研究相關指導原則等要求開展研究,并按照現行藥品注冊管理有關規定執行。”
?海藻糖作為藥用輔料已收載于2015年版中國藥典。在產品質量要求不變的情況下,其供應商的變更應屬于影響較小的變更。然而,變更究竟走備案還是變更申請還與登記狀態有關。
?1.狀態為A的
?表明該產品已經經過至少一次審評,在給藥途徑和添加量不變的情況下,根據以上變更研究技術指導原則,進行相關研究后,在省局進行備案即可。
?如給藥途徑和添加量與之前關聯制劑不一致的,藥品申請人應自行評估風險,備案或者提出變更補充申請。
?2.狀態為I的
?表明該產品登記公示后尚未通過審評,變更需報補充申請,通過CDE關聯審評審批后方可。
?歡迎來電垂詢海藻糖藥用輔料,AVT海藻糖為無菌級低內毒素海藻糖,注射級別,有登記號!400電話:400-6262 623!
?AVT竭誠為您服務!




 瀏覽器自帶分享功能也很好用哦~
瀏覽器自帶分享功能也很好用哦~




